近日,质量安全所畜产品质量安全与营养创新团队在国际肠道微生物学权威期刊《Gut Microbes》(中科院一区Top,IF5y=13.4)发表了题为“Gut bacteriophages induce specific-reprogramming of macrophages to generate a protective innate immunity response to lipopolysaccharide exposure”的重要研究成果。该研究首次发现肠道噬菌体通过诱导巨噬细胞形成“耐受性免疫记忆”,显著抑制LPS刺激下的促炎细胞因子(如IL-6、TNF-α)表达,同时增强了防御性基因簇的应答,减少过度炎症反应,显著提高LPS诱导的急性炎症模型小鼠的存活率。研究成果揭示了肠道噬菌体与机体先天性免疫系统的作用新机制,为开发基于免疫调控的噬菌体治疗策略提供了理论支撑。侯翔博士为论文第一作者,王冉研究员和张莉莉研究员为共同通讯作者。江苏省农业科学院为唯一通讯单位。该研究得到了国家重点研发计划和江苏省农业科技自主创新资金等项目的支持。
巨噬细胞作为先天免疫系统的关键效应细胞,在宿主防御和免疫稳态调控中发挥着核心作用。近年来,噬菌体与先天免疫系统之间的互作机制研究已成为国际前沿热点,特别是在噬菌体治疗领域,其免疫调控机制尚存在诸多亟需解决的科学问题,这些关键问题的突破将直接决定噬菌体治疗的临床效果。
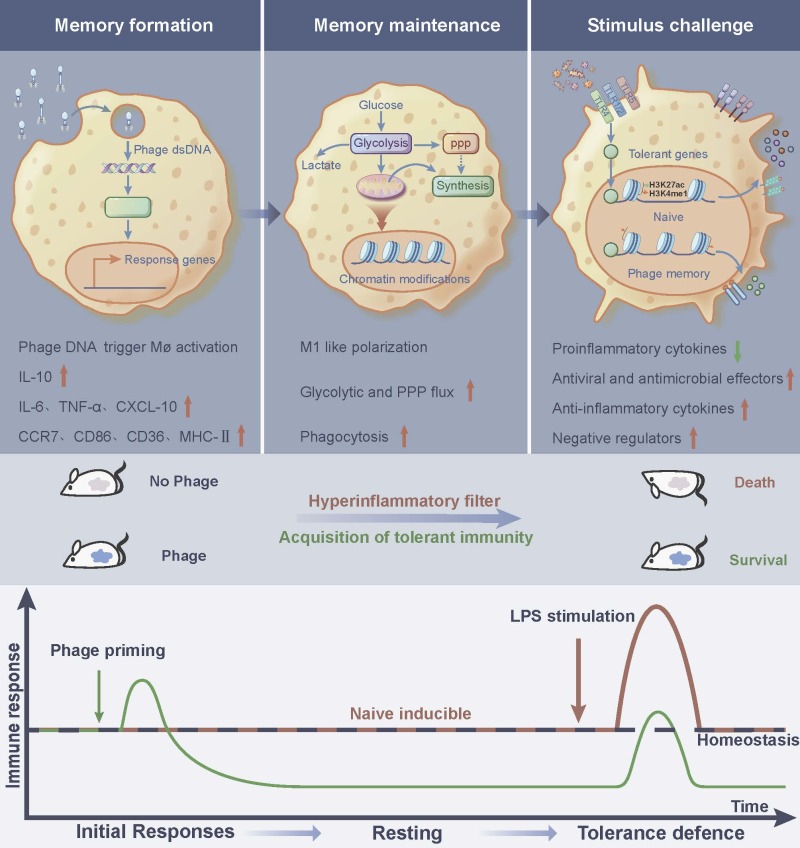
本研究团队揭示了肠道噬菌体调控巨噬细胞免疫应答的多维机制:一方面噬菌体诱导巨噬细胞表型极化转变、显著增强其吞噬功能、并通过重编程代谢网络促进抗菌代谢物衣康酸的积累;另一方面,在表观遗传层面,噬菌体通过选择性抑制组蛋白乙酰化修饰,降低促炎基因位点的染色质可及性,从而在转录水平有效抑制LPS诱导的过度炎症反应,同时特异性激活抗炎和宿主防御相关基因的表达。此外,研究发现这一免疫保护效应主要依赖于白细胞介素-10(IL-10)的特异性高表达,而非简单的促炎因子抑制。该研究不仅阐明了噬菌体-免疫系统互作的新机制,更为噬菌体治疗中免疫平衡的精准调控和免疫稳态的重建提供了重要的理论依据和实践指导。